Содержание
Кремний (Si)

Кремний – самый распространенный электроположительный элемент на Земле. Это полуметалл с характерным металлическим блеском, очень хрупкий. Обычно четырехвалентен в своих соединениях, хотя иногда бывает двухвалентным. Кроме того, известны соединения пятивалентного и шестивалентного кремния.
Кремний занимает 27,72% твердой коры Земли. Следующий элемент после кремния, алюминий составляет 8,13% твердой земной коры.
Природный кремний содержит 92,2% изотопа Si-28, 4,7% Si-29 и 3,1% Si-30. Помимо этих постоянных природных изотопов известны различные искусственные радиоактивные изотопы. Элементный кремний имеет физические свойства полуметаллов, аналогичные свойствам германия и элементов 4-й основной группы. Кремний – полупроводник в чистом виде, хотя интенсивность полупроницаемости значительно увеличивается при добавлении небольших количеств примесей. По своим химическим свойствам похож на металлы.
Кремний почти такой же электроположительный, как олово, и гораздо более положительный, чем германий или свинец. В соответствии с этими металлическими свойствами он образует четырехкратные положительные ионы и различные ковалентные связи. Он появляется как отрицательный ион только в некоторых силицидах и как положительный компонент оксидных кислот или сложных анионов. Образует различные гидриды, галогениды (многие из которых содержат кремниевые соединения) и многие соединения, содержащие кислород, который может иметь ионный или ковалентный характер.
Кремний содержится во многих формах диоксида и в бесчисленных вариациях природных соединений кремнезема.
Применение
Элементарный неочищенный кремний и его полупроводниковые соединения добавляются в сплавы, чтобы сделать металлы, такие как алюминий, магний, медь и другие металлы, более стойкими.
Металлургический кремний чистотой 98-99% используется в качестве сырья для производства кремнийорганических и силиконовых смол и масел. В интегральных схемах используются кремниевые чипы. Фотоэлементы для прямого преобразования солнечной энергии используют тонкие пластинки простых кристаллов кремния. Диоксид кремния используется в качестве сырья для производства элементарного кремния и карбида кремния. Большие кристаллы кремния используются для изготовления пьезоэлектрических стекол. Из расплавленного кварцевого песка получают силиконовые стекла, которые используются в лабораториях и на химических предприятиях, а также для электроизоляции. Коллоидная дисперсия кремния в воде используется в качестве покрывающего агента и как компонент для некоторых эмалей.
В строительной отрасли используются соединения кремния в виде песка и цемента, силиката кальция. Производство стекла и фарфора также основано на песке. Кремний используется в качестве сырья в сталелитейной, химической и электронной промышленности, где он обрабатывается при высоких температурах.
Промышленно важными соединениями кремния являются также силиконы, резина или подобные смолам вещества, которые известны своими водоотталкивающими свойствами и устойчивостью к процессам окисления и химическим воздействиям. Они используются в качестве смазочных материалов при высоких температурах, в качестве уплотнений вокруг окон, крыш или труб, в резиновых шлангах и пластмассовых деталях, например, в автомобильных двигателях, а также в виде силиконовых масел в косметике и средствах по уходу за волосами или для пропитки текстиля.
Карбид кремния почти такой же твердый, как алмаз, используется в качестве абразива. Кристаллы кварца, как природного, так и искусственного происхождения, обладают свойством вибрировать с очень точными частотами при воздействии электрического тока. Это свойство полезно для часов, радио и телевизоров. Жидкое стекло (силикат натрия) используется в чистящих средствах, клеях и отбеливателях для текстильных изделий.
Цеолиты, силиконы, которые используются в качестве регуляторов пенообразования в моющих средствах, напрямую влияют на качество воды. Другие соединения кремния могут действовать как адсорбенты.
Воздействие кремния на здоровье
Элементарный кремний – инертный материал, который может вызывать фиброз легких. Однако сообщалось только о незначительных повреждениях легких лабораторных животных от интратрахеальных инъекций кремниевой пыли. Кремниевая пыль оказывает очень незначительное неблагоприятное воздействие на функцию легких и не вызывает каких-либо серьезных органических заболеваний или токсических эффектов, если уровень воздействия ниже предельных значений.
Кристаллический кремний (диоксид кремния) представляет большую опасность для органов дыхания, однако вероятность повреждения во время производства и нормальной обработки кристаллического кремния очень мала. Пыль с кристаллами кремния при контакте раздражает кожу и глаза. Вдыхание вызывает воспаление легких и слизистых оболочек. Воспаление глаз проявляется слезотечением и покраснением. Покраснение, зуд и сыпь являются симптомами воспаления кожи.
Рак легких напрямую связан с воздействием кристаллов кварца. Причинно-следственная связь была доказана исследованиями горняков, рабочих, работающих на диатомовых землях, рабочих по обработке гранита, рабочих обжига кирпича и других. Некоторые эпидемиологические исследования статистически сообщают о значительном увеличении числа смертей или случаев иммунологических расстройств и аутоиммунных заболеваний у рабочих, подвергшихся воздействию кремния. Эти заболевания и расстройства включают склеродермию, ревматоидный артрит, красную волчанку и саркоидоз.
Кристаллический кремний может атаковать иммунную систему и привести к микробным или грибковым инфекциям (туберкулезу), особенно у рабочих с силикозом. Профессиональное воздействие вдыхаемого кристаллического силикона, среди прочего, является причиной бронхита, хронических стрессовых заболеваний легких и эмфиземы. Некоторые эпидемиологические исследования показывают, что эти последствия для здоровья могут быть менее распространены или отсутствовать у некурящих людей.
Воздействие кремния на окружающую среду
Кремний или его соединения не наносят вред окружающей среде.
Кремний и вода
После кислорода кремний является вторым по распространенности элементом на Земле. В огромных количествах он содержится в различных минералах, а также в виде кремнезема в Мировом океане и во всех других водоемах.
Верхние слои воды океанов содержат около 30 частей кремния на миллион, тогда как более глубокие слои морской воды содержат около 2 частей. В растворенном виде кремний обычно присутствует в виде ортокремниевой кислоты (H4SiO4 или Si(OH)4). Это соединение является результатом медленного растворения силикатов в воде.
Огромное количество частиц кремнезема (оксида кремния) переносится в моря и океаны через реки. Вероятно, менее 20% растворенного кремния снова извлекается из раствора речной воды с помощью биологических и / или химических процессов.
Как и в каких соединениях кремний реагирует с водой?
Кремний никогда не встречается в природе несвязанным. Кроме того, он относительно инертен в своей кристаллической форме, если не подвергается воздействию очень высоких температур. Вода и пар, вероятно, также не имеют большого эффекта, потому что на поверхности очень быстро образуется защитный слой диоксида кремния.
Однако есть также примеры соединений кремния, которые реагируют с водой. Тетрафторид кремния гидролизуется водой с образованием плавиковой кислоты. Тетрахлорид кремния очень бурно реагирует с водой. Силициды первой и второй основной группы более реакционноспособны, чем силициды переходных металлов.
Растворимость кремния и / или его соединений в воде
Соединения кремния могут иметь разную растворимость. Оксид кремния менее растворим в воде, чем другие минералы. Диоксид кремния имеет растворимость в воде 0,12 г / л, тогда как карбид кремния, например, нерастворим в воде.
Как кремний может попасть в воду?
Как уже упоминалось, кремний содержится во многих минералах, из которых он может быть растворен в результате процессов выветривания. Он также выделяется во время вулканической активности под водой. Вода в пустотах морских отложений содержит больше кремния, чем верхние слои морской воды.
С другой стороны, кремний удаляется из воды естественным путем. Это может произойти из-за фиксации планктоном в океанах, осаждения отложений или реакций растворенного кремния с глиной в отложениях (обратное выветривание). Минералы, такие как тальк, слюда, полевой шпат, нефелин, оливин, вермикулит, перлит и каолинит, также содержат кремний. То же самое относится к таким драгоценным камням, как опал или аметист.
Какие экологические проблемы может вызвать загрязнение воды кремнием?
Диоксид кремния необходим для некоторых организмов, но до сих пор неясно, как он попадает в них. Диатомовые водоросли, радиолярии и губки нуждаются в нем для своего скелета, а иголки различных видов крапивы сделаны из этого вещества. Курам и крысам кремний нужен для роста костей, и, по-видимому, он также важен для человека, где он в основном содержится в соединительной ткани и коже.
Кремний также необходим для роста растений. Различные виды растений содержат элемент в количестве 200-62000 частей на миллион (в пересчете на сухое вещество). Такие растения, как хвощ и бамбук, содержат оксид кремния в стеблях и листьях, что придает им дополнительную стабильность.
Поскольку он естественным образом содержится в больших количествах в воде, кремний фактически считается безвредным. Кремний в природе встречается в форме трех разных изотопов, ни один из которых не является радиоактивным.
Какие последствия для здоровья может вызывать кремний в воде?
Общее количество кремния в организме человека составляет около 1 г и с возрастом уменьшается. Поскольку это важно для роста костей некоторых организмов, считается, что он также необходим и для людей. В основном он содержится в соединительной ткани и коже. Симптомы дефицита кремния неизвестны.
Мелкая пыль от соединений кремния может вызвать силикоз, типичное профессиональное заболевание, например, у шахтеров или камнерезов. Последствиями являются одышка, хрипы и кашель. Однако это происходит только при вдыхании веществ. Есть подозрения, что силиконовые грудные имплантаты вызывают аутоиммунные заболевания и даже рак. Однако научных подтверждений этому нет. Силиконы используются в желудочных таблетках для лечения колик и диареи.
Некоторые соединения кремния, такие как соединения кремний-галоген, обладают коррозионным действием или очень токсичны, например, некоторые органические соединения кремния. Тетрахлорид кремния раздражает глаза, органы дыхания и кожу. Кремнезем обычно присутствует в основном в питьевой воде, но считается безвредным.
Кремний

Кремний (Si от лат. Silicium ) — элемент четырнадцатой группы (по старой классификации — главной подгруппы четвёртой группы), третьего периода периодической системы химических элементов с атомным номером 14. Атомная масса 28,085. Неметалл, второй по распространённости химический элемент в земной коре (после кислорода). Исключительно важен для современной электроники.
Содержание
- 1 История
- 2 Происхождение названия
- 3 Нахождение в природе
- 4 Изотопы и их применение
- 5 Получение
- 6 Физические свойства
- 6.1 Электрофизические свойства
- 7.1 Гибридизация
- 7.2 Малая активность кремния
- 7.3 Реакция с галогенами
- 7.4 Реакция с кислородом
- 7.5 Получение монооксида кремния
- 7.6 Получение силанов
- 7.7 Реакция с азотом и бором
- 7.8 Получение карборунда
- 7.9 Кремний растворяет многие металлы
- 7.10 Силициды
- 7.11 Некоторые кремнийорганические соединения
- 7.12 Травление кислотами
- 7.13 Травление щелочами
- 9.1 В организме человека
История
Существование кремния было предсказано Йёнсом Якобом Берцелиусом в 1810 году. Позже, в 1823 году он выделил аморфный кремний путём восстановления фторида SiF4 калием, подробно описал его химические свойства.
Впервые в чистом виде кремний был выделен в 1811 году французскими учёными Жозефом Луи Гей-Люссаком и Луи Жаком Тенаром.
Происхождение названия
В 1823 году шведский химик Йёнс Якоб Берцелиус действием металлического калия на фтористый кремний SiF4 получил чистый элементарный кремний. Новому элементу было дано название «силиций» (от лат. silex — кремень). Русское название «кремний» введено в 1834 году российским химиком Германом Ивановичем Гессом. В переводе c др.-греч. κρημνός — «утёс, гора».
Нахождение в природе
Содержание кремния в земной коре составляет по разным данным 27,6—29,5 % по массе. Таким образом, по распространённости в земной коре кремний занимает второе место после кислорода. Концентрация в морской воде 3 мг/л.
Чаще всего в природе кремний встречается в виде кремнезёма — соединений на основе диоксида кремния (IV) SiO2 (около 12 % массы земной коры). Основные минералы и горные породы, образуемые диоксидом кремния, — это песок (речной и кварцевый), кварц и кварциты, кремень, полевые шпаты. Вторую по распространённости в природе группу соединений кремния составляют силикаты и алюмосиликаты.
Отмечены единичные факты нахождения чистого кремния в самородном виде.
Изотопы и их применение
Кремний состоит из стабильных изотопов 28 Si (92,23 %), 29 Si (4,67 %) и 30 Si (3,10 %). Остальные изотопы являются радиоактивными.
Ядро 29 Si (как и протон) имеет ядерный спин I = 1/2 и все шире используется в спектроскопии ЯМР. 31 Si, образующийся при действии нейтронов на 30 Si, имеет период полураспада равный 2,62 ч. Его можно определить по характеристическому β-излучению, и он очень удобен для количественного определения кремния методом нейтронно-активационного анализа. Радиоактивный нуклид 32 Si имеет самый большой период полураспада (
170 лет) и является мягким (низкоэнергетическим) β-излучателем.
Получение
Свободный кремний получается при прокаливании мелкого белого песка (диоксида кремния) с магнием:
SiO2 + 2Mg ⟶ 2MgO + Si
При этом образуется аморфный кремний, имеющий вид бурого порошка.
В промышленности кремний технической чистоты получают, восстанавливая расплав SiO2 коксом при температуре около 1800 °C в рудотермических печах шахтного типа. Чистота полученного таким образом кремния может достигать 99,9 % (основные примеси — углерод, металлы).
Возможна дальнейшая очистка кремния от примесей.
- Очистка в лабораторных условиях может быть проведена путём предварительного получения силицида магния Mg2Si. Далее из силицида магния с помощью соляной или уксусной кислот получают газообразный моносилан SiH4. Моносилан очищают ректификацией, сорбционными и др. методами, а затем разлагают на кремний и водород при температуре около 1000 °C .
- Очистка кремния в промышленных масштабах осуществляется путём непосредственного хлорирования кремния. При этом образуются соединения состава SiCl4, SiHCl3 и SiH2Cl2. Их различными способами очищают от примесей (как правило, перегонкой и диспропорционированием) и на заключительном этапе восстанавливают чистым водородом при температурах от 900 до 1100 °C .
- Разрабатываются более дешёвые, чистые и эффективные промышленные технологии очистки кремния. На 2010 г. к таковым можно отнести технологии очистки кремния с использованием фтора (вместо хлора); технологии, предусматривающие дистилляцию монооксида кремния; технологии, основанные на вытравливании примесей, концентрирующихся на межкристаллитных границах.
Содержание примесей в доочищенном кремнии может быть снижено до 10 −8 —10 −6 % по массе. Более подробно вопросы получения сверхчистого кремния рассмотрены в статье Поликристаллический кремний.
Способ получения кремния в чистом виде разработан Николаем Николаевичем Бекетовым.
В России технический кремний производится «ОК Русал» на заводах в г. Каменск-Уральский (Свердловская область) и г. Шелехов (Иркутская область); доочищенный по хлоридной технологии кремний производит группа «Nitol Solar» на заводе в г. Усолье-Сибирское.
Физические свойства
Кристаллическая решётка кремния кубическая гранецентрированная типа алмаза, параметр а = 0,54307 нм (при высоких давлениях получены и другие полиморфные модификации кремния), но из-за большей длины связи между атомами Si—Si по сравнению с длиной связи С—С твёрдость кремния значительно меньше, чем алмаза. Кремний хрупок, только при нагревании выше 800 °C он становится пластичным веществом. Он прозрачен для инфракрасного излучения начиная с длины волны 1,1 мкм. Собственная концентрация носителей заряда — 5,81⋅10 15 м −3 (для температуры 300 K).
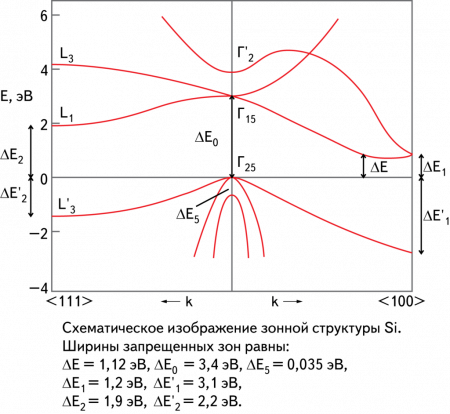
Электрофизические свойства
Элементарный кремний в монокристаллической форме является непрямозонным полупроводником. Ширина запрещённой зоны при комнатной температуре составляет 1,12 эВ, а при Т = 0 К — 1,21 эВ. Концентрация собственных носителей заряда в кремнии при нормальных условиях составляет около 1,5⋅10 10 см −3 .
На электрофизические свойства кристаллического кремния большое влияние оказывают содержащиеся в нём примеси. Для получения кристаллов кремния с дырочной проводимостью в кремний вводят атомы элементов III группы, таких, как бор, алюминий, галлий, индий. Для получения кристаллов кремния с электронной проводимостью в кремний вводят атомы элементов V группы, таких, как фосфор, мышьяк, сурьма.
При создании электронных приборов на основе кремния используется преимущественно приповерхностный слой монокристалла (толщиной до десятков мкм), поэтому качество поверхности кристалла может оказывать существенное влияние на электрофизические свойства кремния и, соответственно, на свойства созданного электронного прибора. При создании некоторых приборов используется технология, модифицирующая поверхность монокристалла, например, обработка поверхности кремния различными химическими реагентами и её облучение.
- Диэлектрическая проницаемость: 12
- Подвижность электронов: 1200—1450 см²/(В·c).
- Подвижность дырок: 500 см²/(В·c).
- Ширина запрещённой зоны 1,21 эВ при 0 К.
- Время жизни свободных электронов: 5 нс — 10 мс
- Длина свободного пробега электронов: порядка 1 мм.
- Длина свободного пробега дырок: порядка 0,2—0,6 мм.
Все значения приведены для нормальных условий.
Химические свойства
Гибридизация
Подобно атомам углерода, для атомов кремния является характерным состояние sp 3 -гибридизации орбиталей. В связи с гибридизацией чистый кристаллический кремний образует алмазоподобную решётку, в которой кремний четырёхвалентен. В соединениях кремний обычно также проявляет себя как четырёхвалентный элемент со степенью окисления +4 или −4. Встречаются двухвалентные соединения кремния, например, оксид кремния (II) — SiO.
Малая активность кремния
При нормальных условиях кремний химически малоактивен и активно реагирует только с газообразным фтором, при этом образуется летучий тетрафторид кремния SiF4.
Такая «неактивность» кремния связана с пассивацией поверхности наноразмерным слоем диоксида кремния, немедленно образующегося в присутствии кислорода, воздуха или воды (водяных паров).
Реакция с галогенами
При нагревании до температуры свыше 400—500 °C кремний реагирует с хлором, бромом и иодом — с образованием соответствующих легко летучих тетрагалогенидов SiHal4 и, возможно, галогенидов более сложного состава.
Реакция с кислородом
При нагревании до температуры свыше 400—500 °C кремний реагирует с кислородом с образованием диоксида SiO2.
Процесс сопровождается увеличением толщины слоя диоксида на поверхности, скорость процесса окисления лимитируется диффузией атомарного кислорода сквозь плёнку диоксида.
Получение монооксида кремния
При восстановлении SiO2 кремнием при температурах свыше 1200 °C образуется оксид кремния (II) — SiO.
Si + SiO2 → t>1200oC 2SiO
Этот процесс постоянно наблюдается при производстве кристаллов кремния методами Чохральского, направленной кристаллизации, потому что в них используются контейнеры из диоксида кремния, как наименее загрязняющего кремний материала.
Получение силанов
С водородом кремний непосредственно не реагирует. Cоединения кремния с водородом — силаны с общей формулой SinH2 n+2 — получают косвенным путём. Моносилан SiH4 (его часто называют просто силаном) выделяется при взаимодействии силицидов металлов с растворами кислот, например:
Образующийся в этой реакции силан SiH4 содержит примесь и других силанов, в частности, дисилана Si2H6 и трисилана Si3H8 , в которых имеется цепочка из атомов кремния, связанных между собой одинарными связями ( −Si−Si−Si− ).
Реакция с азотом и бором
С азотом и бором кремний реагирует при температуре около 1000 °C , образуя соответственно нитрид Si3N4 и термически и химически стойкие бориды SiB3, SiB6 и SiB12.
Получение карборунда
При температурах свыше 1000 °C можно получить соединение кремния и его ближайшего аналога по таблице Менделеева — углерода — карбид кремния SiC (карборунд), который характеризуется высокой твёрдостью и низкой химической активностью.
Si + C → t>1000oC SiC
Карборунд широко используется как абразивный материал. При этом, что интересно, расплав кремния ( 1415 °C ) может длительное время контактировать с углеродом в виде крупных кусков плотноспечённого мелкозернистого графита изостатического прессования, практически не растворяя и никак не взаимодействуя с последним.
Кремний растворяет многие металлы
Нижележащие элементы 4-й группы (Ge, Sn, Pb) неограниченно растворимы в кремнии, как и большинство других металлов.
Силициды
При нагревании кремния с металлами могут образовываться их соединения — силициды.
Силициды можно подразделить на две группы: ионно-ковалентные (силициды щелочных, щелочноземельных металлов и магния типа Ca2Si, Mg2Si и др.) и металлоподобные (силициды переходных металлов). Силициды активных металлов разлагаются под действием кислот, силициды переходных металлов химически стойки и под действием кислот не разлагаются. Металлоподобные силициды имеют высокие температуры плавления (до 2000 °C ). Наиболее часто образуются металлоподобные силициды составов MeSi, Me3Si2, Me2Si3, Me5Si3 и MeSi2. Металлоподобные силициды химически инертны, устойчивы к действию кислорода даже при высоких температурах.
Особо следует отметить, что с железом кремний образует эвтектическую смесь, что позволяет спекать (сплавлять) эти материалы для образования ферросилициевой керамики при температурах, заметно меньших, чем температуры плавления железа и кремния.
Некоторые кремнийорганические соединения
Для кремния характерно образование кремнийорганических соединений, в которых атомы кремния соединены в длинные цепочки за счёт мостиковых атомов кислорода −O− , а к каждому атому кремния, кроме двух атомов O , присоединены ещё два органических радикала R1 и R2=CH3 , C2H5 , C6H5 , CH2CH2CF3 и др.
Травление кислотами
Для травления кремния наиболее широко используют смесь плавиковой и азотной кислот. Некоторые специальные травители предусматривают добавку хромового ангидрида и иных веществ. При травлении кислотный травильный раствор быстро разогревается до температуры кипения, при этом скорость травления многократно возрастает.
- Si + 2HNO3 = SiO2 + NO + NO2 + H2O
- SiO2 + 4HF = SiF4 + 2H2O
- 3SiF4 + 3H2O = 2H2SiF6 + H2SiO3↓
Травление щелочами
Для травления кремния могут использоваться водные растворы щёлочей. Травление кремния в щелочных растворах начинается при температуре раствора более 60 °C .
- Si + 2KOH + H2O = K2SiO3 + 2H2↑
- K2SiO3 + 2H2O ↔ H2SiO3 + 2KOH
Применение

Технический кремний находит следующие применения:
- сырьё для металлургических производств: компонент сплава (бронзы, силумин); раскислитель (при выплавке чугуна и сталей); модификатор свойств металлов или легирующий элемент (например, добавка определённого количества кремния при производстве трансформаторных сталей уменьшает коэрцитивную силу готового продукта) и т. п.;
- сырьё для производства более чистого поликристаллического кремния и очищенного металлургического кремния (в литературе «umg-Si»);
- сырьё для производства кремнийорганических материалов, силанов;
- иногда кремний технической чистоты и его сплав с железом (ферросилиций) используется для производства водорода в полевых условиях;
- для производства солнечных батарей;
- антиблок (антиадгезивная добавка) в промышленности пластмасс.

Сверхчистый кремний преимущественно используется для производства одиночных электронных приборов (нелинейные пассивные элементы электрических схем) и однокристальных микросхем. Чистый кремний, отходы сверхчистого кремния, очищенный металлургический кремний в виде кристаллического кремния являются основным сырьевым материалом для солнечной энергетики.
Монокристаллический кремний — помимо электроники и солнечной энергетики, используется для изготовления зеркал газовых лазеров.
Соединения металлов с кремнием — силициды — являются широко употребляемыми в промышленности (например, электронной и атомной) материалами с широким спектром полезных химических, электрических и ядерных свойств (устойчивость к окислению, нейтронам и др.). Силициды ряда элементов являются важными термоэлектрическими материалами.
Соединения кремния служат основой для производства стекла и цемента. Производством стекла и цемента занимается силикатная промышленность. Она также выпускает силикатную керамику — кирпич, фарфор, фаянс и изделия из них.
Широко известен силикатный клей, применяемый в строительстве как сиккатив, а в пиротехнике и в быту для склеивания бумаги.
Получили широкое распространение силиконовые масла и силиконы — материалы на основе кремнийорганических соединений.
Биологическая роль
Для некоторых организмов кремний является важным биогенным элементом. Он входит в состав опорных образований у растений и скелетных — у животных. В больших количествах кремний концентрируют морские организмы — диатомовые водоросли, радиолярии, губки. Большие количества кремния концентрируют хвощи и злаки, в первую очередь — подсемейства Бамбуков и Рисовидных, в том числе — рис посевной.
Он также используется для создания клеточных стенок некоторых организмов и является центром реактивности дюжины или около того ферментов, ответственных за «обработку» диатомового кремнезема y некоторых ракообразных.
Кремний встречается во многих растениях, которые необходимы для правильного развития, но не было доказано, что это необходимо для развития всех видов. Обычно его присутствие повышает устойчивость к вредителям, особенно грибам, препятствует их проникновению в ткани растений, насыщенных кремнеземом. Точно так же в случае животных необходимость в кремнии была продемонстрирована для шестилучевых губок, но, хотя это происходит в телах всех животных, это, как правило, не оказывается необходимым для них. У позвоночных это происходит в больших количествах в волосах и перьях (например, овечья шерсть содержит 0,02—0,08 % SiO2 ). Мышечная ткань человека содержит (1—2)⋅10 −2 % кремния, костная ткань — 17⋅10 −4 % , кровь — 3,9 мг/л . С пищей в организм человека ежедневно поступает до 1 г кремния.
В организме человека
Доказано, что кремний имеет важное значение для здоровья человека, в частности, для ногтей, волос, костей и кожи. Исследования показывают, что женщины в пременопаузе с более высоким потреблением биодоступного кремния имеют более высокую плотность костной ткани, а также, что добавки кремния может увеличить объем и плотность кости у пациентов с остеопорозом.
Организм человека нуждается в 20—30 мг кремния в день. Беременным женщинам, людям после операций на костях и пожилым людям требуется более высокая доза, так как количество этого элемента в органах уменьшается с возрастом. Это происходит главным образом в соединительной ткани, из которой строятся сухожилия, слизистые оболочки, стенки кровеносных сосудов, клапаны сердца, кожа и костно-суставная система. Кремний удаляет токсичные вещества из клеток, предпочтительно воздействует на капилляры, герметизирует их, повышает прочность костной ткани, укрепляет защитные силы организма от инфекций, предотвращает преждевременное старение. Снимает раздражения и воспаления кожи, улучшая её общий вид и предотвращая вялость, уменьшает выпадение волос, ускоряет их рост, укрепляет ногти. Поскольку кремний участвует в формировании костной ткани, обеспечивая эластичность кровеносных сосудов, участвующих в поглощении кальция из рациона и роста волос и ногтей, его дефицит в организме человека может вызвать костные аномалии, общее замедление роста, бесплодие, отсутствие развития и остеопороз. Диоксид кремния в нормальных условиях всегда является твёрдым биоинертным, неразлагаемым веществом, склонным к образованию пыли, состоящей из частиц с острыми режущими кромками. Вредное действие диоксида кремния и большинства силицидов и силикатов основано на раздражающем и фиброгенном действии, на накоплении вещества в ткани лёгких, вызывающем тяжёлую болезнь — силикоз. Для защиты органов дыхания от пылевых частиц используются противопылевые респираторы. Тем не менее, даже при использовании средств индивидуальной защиты носоглотка, горло у людей, систематически работающих в условиях запыленности соединениями кремния и особенно монооксидом кремния, имеют признаки воспалительных процессов на слизистых оболочках. Нормы предельно допустимых концентраций по кремнию привязаны к содержанию пыли диоксида кремния в воздухе. Это связано с особенностями химии кремния:
Кремний (Si) – роль в организме, симптомы недостатка, источники
Кремний (Silicium, Si) – химический элемент и микроэлемент для человеческого организма, без которого некоторые формы жизни, например, губки и диатомеи вообще не могут существовать, ведь именно кремний является одним из важнейших строительных элементов костной ткани. Да-да, мы привыкли, что кости – это «кальций», но это скорее всего знания из рекламы, т.к. для формирования и развития костей необходимо множество разных веществ, и кремний – один из них.

Кроме того, кремний играет важную роль в поддержании здоровья кожи, волос и ногтей. За счет этого, недостаток кремния в организме человека проявляется, главным образом, сухими и секущимися волосами, повышенной ломкостью ногтей, дряблой кожей и склонностью к переломам. А еще, Si повышает эластичность и прочность кровеносных сосудов, чем минимизирует развитие сердечно-сосудистых болезней.
Наиболее же известным для многих людей применением кремния является производство микрочипов – процессоров, чипсетов и прочих радиодеталей. Собственно, и сам научный т.н. центр по компьютерным разработкам находится в одноименной точке – «Кремниевая долина» (Калифорния, США).
В природе, кремний чаще всего встречается в форме диоксида кремния (SiO2), который в сочетании с другими минералами образовывает соединения под названием – «кремнезём» или «силикаты». Кремнезём же может быть строительным материалом для кремня, кварца, полевого шпата и прочих. В очень редких случаях в руки ученым попадались небольшие экземпляры чистого кремния.
Обратите внимание, что кремний и кремень – разные понятия, которые не стоит путать. Кремень является камнем, горной породой, в составе которого присутствует диоксид кремния (SiO2) и могут присутствовать другие химические элементы – кальций, медь, марганец, фосфор, цинк, стронций и прочие. Таким образом, кремень – это камень, состоящий из разных элементов, а кремний – химический элемент. Вроде звучит банально, но отличие важное.

Еще интересным фактов является количество Si на Землей! Задумайтесь, количество кремния в земной коре (кларк) по разным данным составляет от 27,6 до 29,5% всей массы! 1 В итоге, получается, что больше на Земле только кислорода (О), а Si идет сразу же за ним. В самой только морской воде этого химического элемента находится в пределах 3 мг на 1л.
Самородный кремний в природе представляет собой непрозрачный неметалл темно-серого цвета с металлическим блеском.
Свое наименование «Silicium (силициум)» кремний получил от латинского слова «silex», что в переводе означает — камень, скала, утес. Русский же термин «кремний» этот химический элемент получен в 1834 году русским химиком Германом Гессом от старославянского «кремень», означающий — твердый камень.
История – краткая справка
Первые сведения о кремнии появились в начале 18 ст., когда химик из Швеции Йенс Якоб Берцелиус в 1810 году заявил о наличии нового, до селе неописанного наукой элементе, однако, в чистой форме ученый смог выделить Si а ж в 1823 году. Именно тогда новый элемент получилось получить от обработки калиевой соли с помощью металлического калия и фтористого кремния под нагревом до высоких температур. Тогда же ему и присвоили наименование «Силиций».
Несколькими годами ранее, в 1811 году Si в чистом виде удалось добыть 2 учеными из Франции, которых звали Луи Жак Тенар и Жозеф Луи Гей Люссак.
Общие данные
Расположение в периодической таблице Д.И. Менделеева: в старой версии — III период, III ряд, IV группа, в новой версии таблицы – 14 группа, 3 период.
- Атомный номер – 14
- Атомная масса – 28,086 а. е. м.
- Электронная конфигурация – [Ne] 3s2 3p2
- Температура плавления (°С) – 1414,85 (1688 K)
- Температура кипения (°С) – 2349,85 (2623 К).
- CAS: 7440-21-3.
Физико-химические свойства. Физические и химические свойства кремния зависят от его формы.
Кристаллический кремний представляет собой хрупкое, но в то же самое время очень твердое кристаллическое вещество темно-серого цвета с металлическим отблеском.
Аморфный кремний представляет собой порошкообразное вещество бурого цвета.
Под воздействием высоких температур (от 800 °С) Si становится пластичным. Несмотря на отсутствие прозрачности, спокойно пропускает через себя инфракрасный спектр лучей, длина которых составляет от 1.1 микрометра.Химически Si – малоактивный элемент. При температуре в пределах 21-24 °С реагирует с фтором (F), образовывая летучий тетрафторид кремния SiF4. При воздействии более высоких температур, от 400 до 500 °C начинает реагировать с кислородом (О), образовывая диоксид кремния, а также с бромом (Br), хлором (Cl) и йодом (I) – летучие тетрагалогениды (SiHal4). При температуре 1000 °C уже вступает в реакцию с азотом, образовывая нитрид азота Si3N4, или бориды (SiB3, SiB6, SiB12) при контакте с бором. А вот с водородом Si не реагирует.
Si растворяется в горячих щелочных растворах.
Биологическая роль и функции кремния в организме

Для чего нужен кремний организму? Как мы уже и говорили в начале статьи, Si играет важную роль в формировании и поддержании здоровья костной ткани, кожного покрова, волос, ногтей, а также кровеносных сосудов.
Количество кремния в костных тканях взрослого среднестатистического человека 17⋅10−4 %, в мышечных тканях — (1-2)⋅10−2 %, в крови — 3,9 мг/л, а также гипофизе, щитовидной железе, надпочечниках, ногтях и волосах.
В нашем организме кремний больше всего содержится в щитовидной железе, надпочечниках, гипофизе. Самая высокая концентрация его обнаружена в волосах и ногтях.
Кремний выполняет и множество других полезных функций, среди которых:
- Делает кости более плотными, что особенно важно для женщин в период климакса, когда продукция некоторых гормонов снижается и появляется риск развития остеопороза (процесс, при котором снижается плотностей костей). Таким образом, дополнительный прием кремния рекомендуется лицам, у которых уже диагностирован остеопороз.
- Ускоряет процесс выздоровления и восстановления организма после оперативного лечения костей – после переломов и прочих хирургических манипуляций.
- Является одним из важных строительных элементов коллагена, причем, находясь в составе этого белка соединительной ткани, кремний участвует в процессе соединения отдельных волокон коллагена с эластином, за счет чего соединительная ткань становится упругая и прочная.
- Находясь в составе эластина, повышает эластичность и прочность кровеносных сосудов, чем предупреждает проникновение в кровеносное русло жиров и образование атеросклеротических отложений и связанных с ними болезней (инфаркта, инсульта, ИБС, тромбофлебита и прочих).
- Задействован в укреплении хрящей, связок и сухожилий.
- Участвует в регулировании деятельности иммунной системы, тем самым минимизирует риск развития инфекционных болезней.
- Поддерживает здоровье кожи и помогает бороться с дерматитами, дерматозами и прочими воспалительными процессами на кожном покрове.
- Укрепляет волосы, предотвращает их сечение и выпадение, а также стимулирует рост волос.
- За счет создания электрических коллоидных систем с водой и кремниевой кислотой Si способствует связыванию болезнетворных микроорганизмов (вирусов, бактерий) и выведению их из внутренней среды человека, т.е. грубо говоря, выступает в качестве сорбента.
- Берет участие в метаболизме магния, калия, фтора, алюминия и прочих макро- микроэлементов.
- Участвует в синтезе различных гормонов, аминокислот, ферментов.
- Предотвращает преждевременное старение организма.
- Усиливает антиоксидантную активность витаминов А, С и Е, чем предотвращает развитие онкологических болезней.
- Находясь в воде, кремний адсорбирует радионуклиды, способствует выпадению в осадок тяжелых металлов, уничтожает бактерии, вызывающих гниение воды. Именно из-за этих свойств, этот минерал используют для очищения воды, более того, Si даже делает воду более приятной на вкус.
Применение кремния в других сферах человеческой жизни
- Прежде всего, Si используют в качестве полупроводников для изготовления электроники, особенно микрочипов, транзисторов, диодов, солнечных панелей и прочих.
- В металлургии он пользуется успехом в качестве дополнительного материала в сплавах меди, алюминия, магния и прочих металлов, предавая сплавам более высокую прочность.
- Его добавляют в производстве кремнийорганических соединений – для изготовления пластика, искусственного каучука, технических силикатных смазок и масел.
- Используется и для производства неорганических материалов – керамики, стекла, изоляции, пьезокристаллов.
- В медицинской практике – для лечения остеопороза.
Кремний — суточная потребность
Суточная потребность в кремнии среднестатистического взрослого человека составляет 5 мг 2 . Максимальная суточная доза в Si – 10 мг. Хотя, некоторые источники утверждают, что суточная доза Silicium должна составлять от 20 до 50 мг.
Суточная доза кремния повышается при беременности, пременопаузе, после хирургического лечения, при переломах, высоких физических нагрузках на организм.
Терапевтической дозой кремния является до 12 мг в сутки 3 .
Нехватка кремния — симптомы
Дефицит Si может вызывать следующие нарушения в работе организма:
- Дряблость и сухость кожи, а также склонность к рецидивирующим кожным болезням – экземе, дерматиту, дерматозу, рожистым воспалениям и прочим. Раны заживают медленнее;
- Волосы становятся тусклыми, секутся и выпадают в повышенном количестве;
- Ногти также становятся более ломкими, периодически слоятся;
- Со временем развивается остеомаляция костей (размягчение костной ткани), остеопороз, артриты, склонность к переломам;
- Появляется ряд зубных болезней – кариес, пародонтоз;
- Развивается ряд заболеваний сердца и сосудов – артериальная гипертензия (гипертония), атеросклероз, ишемическая болезнь сердца, тромбофлебит, варикозное расширение вен, склонность к инфаркту и инсульту;
- Снижение аппетита;
- Повышенное утомление, периодическая слабость и апатия;
- Склонность к инфекционным болезням;
- Замедление роста ребенка;
- Бесплодие;
- Сосуды теряют свою эластичность, из-за чего при небольшом ушибе на коже появляются синяки, а также периодическое формирование сосудистых «звездочек».
- Кроме того, замечена связь между недостаточным количеством кремния в организме и наличием в это время следующих болезней – катаракта, сахарный диабет, дисбактериоз, гепатит, наличие камней в желчном пузыре (ЖКБ) и почках (ПКБ), злокачественные опухоли (рак).
Причины нехватки Si
- Недостаточное поступление микроэлемента из-за недостаточного питания, жестких и несбалансированных диет, голодовки;
- Употребление продуктов питания, скудных на полезные вещества – малополезной и вредной пищи; ;
- Наличие в организме глистных инвазий и прочих паразитов.
Применение кремния в медицине
Применение Silicium целесообразно в следующих случаях:
- Восстановление организма после оперативного лечения хирургическим путем;
- Профилактика остеопороза;
- Восстановление здоровья волос, ногтей, кожи.
Избыток кремния
Передозировка этим полезным микроэлементов также возможна.
Отравление кремнием сопровождается следующими симптомами:
- Учащенное мочеиспускание, что приводит к повышенному вымыванию кальция из организма и соответственно делает кости более ломкими;
- Формирование камней в желчном пузыре, мочевом пузыре и почках, из-за чего у человека появляются периодические боли при мочеиспускании;
- Резкое снижение уровня сахара в крови при сахарном диабете;
- Повышенный уровень сахара в крови.
Причины переизбытка Si в организме
Злоупотребление препаратами, в которых содержится этот химический элемент;
Работа на производстве по обработке кремня – пылевые частицы с кремнием попадают на слизистые дыхательных путей и пищеварительного тракта, вызывая в местах оседания воспалительные процессы, а также развитие силикоза.
Источники кремния

В каких продуктах кремний содержится больше всего?
Растительные и животные источники (мг на 100 г): рис (1240), овес (1000), просо (754), ячневая крупа (600), кунжутное семя (200), соя (177), гречка (120), земляника (100), ананас (94), фасоль (92), репа (90), жимолость (90), горох (84), дыня (81), чечевица (80), свекла (80), банан (75), авокадо (65), кукуруза (60), грецкий орех (58), капуста белокочанная (55), огурцы (50), картофель (50), фисташки (50), пшеница (48), инжир свежий (48), вишня (46), овсянка (43), шпинат (42), малина (40), редька (40), редис (30), петрушка (30), сельдерей (29), морковь (25), перец болгарский (22), черника (20), виноград (12), персик (10), помидоры (10), апельсин (6), груша (6), абрикос (6), слива (4), хвощ полевой (2,5).
Дополнительным источником Si могут стать минеральные воды.
Химические источники (Si): «Кремний активный» (таблетки), MSM комплекс в составе БАДов.
Синтез в организме: не синтезируется.
Взаимодействие кремния с другими веществами
- Усиливает антиоксидантную активность витаминов А, Е и С;
- Улучшает усвоение следующих макро- и микроэлементов – кальция, калия, магния, натрия, фосфора, фтора и серы;
- Является антагонистом молибдена, из-за чего при их одновременном применении, активность обоих снижается. Кроме того, прием повышенных дох молибдена снижает усвояемость кремния;
- При взаимодействии с алюминием и марганцем образовывает нерастворимые силикаты, которые могут оседать в организме;
- Нейтрализует вредное действие на организм нитратов, солей свинца, хлор, ртути и прочих тяжелых металлов.
Видео
Обсудить S и другие минералы на форуме…
Источники:
1. «Обилие химических элементов в Земной коре: новая таблица». Автор: Taylor S.R., Журнал «Геохимия и Космохимия» 29 том, №8, 1964 г. Страницы 1273—1285.
2. Методические рекомендации Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека №2.3.1.1915-04 от 02.07.2004.
Источник https://snab365.ru/silicon/
Источник https://chem.ru/kremnij.html
Источник https://medicina.dobro-est.com/kremniy-si-rol-v-organizme-simptomyi-nedostatka-istochniki.html